Transwell细胞体外侵袭实验
应用于各种细胞因子对恶性肿瘤细胞侵袭和转移的影响及一些抑制血管生成的新药研究
Transwell细胞体外侵袭实验是一种通过聚碳酸酯膜分隔培养装置的体外检测模型,主要用于评估恶性肿瘤细胞的侵袭转移能力及抗血管生成药物筛选。该实验通过在小室上室侧铺基质胶模拟体内细胞外基质环境,利用下室趋化因子诱导细胞迁移,侵袭测定要求细胞分泌基质金属蛋白酶(MMPs)降解基质胶后方可通过膜结构。实验中采用无血清饥饿处理细胞悬液后接种至上室,下室填充含胎牛血清或趋化因子的培养基,通过直接计数法(结晶紫染色)或间接计数法(MTT法)检测穿过膜的细胞数量 [1]。改进方法优化了趋化因子制备流程,将实验周期压缩至2天,关键控制点包括使用对数生长期细胞(活力>95%)、规范苏木素染色时间(新染液1分钟,重复使用2分钟)。
产品介绍
目的:总结并改进细胞体外侵袭实验的操作经验。结果:改进后侵袭试验定位准确,结果清晰。结论:按照作者建议的方法操作,能够缩短实验时间,有助于提高细胞体外侵袭实验的质量。/p>
细胞体外侵袭实验主要应用于各种细胞因子对恶性肿瘤细胞侵袭和转移的影响及一些抑制血管生成的新药研究,但在具体实验中获得真实、最佳实验结果的图像,并借以说明问题并非简单。
很多研究人员在此方面花费了很多时间和科研经费,从刺激实验用的细胞到苏木素染色,看似简单的实验步骤中有很多环节需要研究者注意.
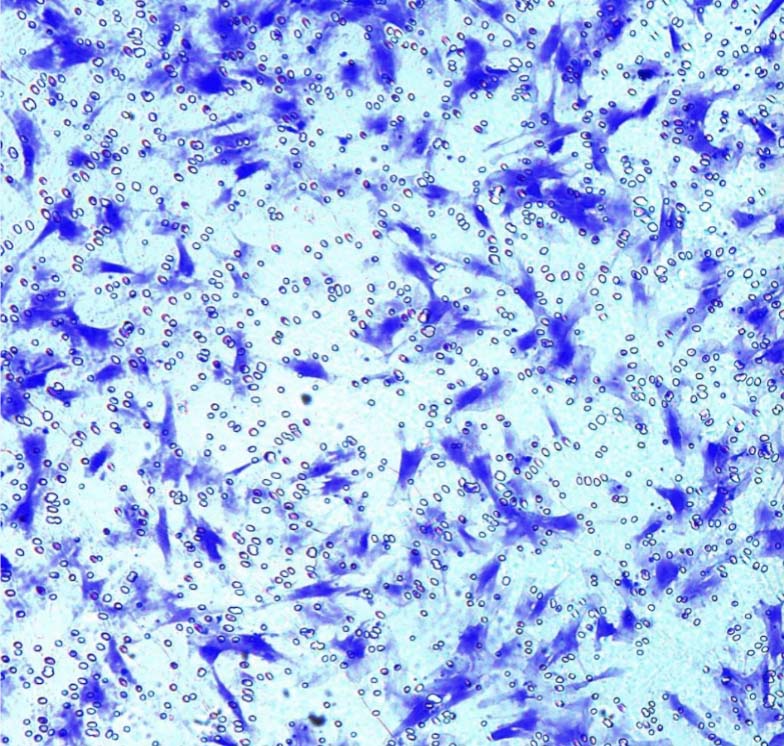
细胞迁移
材料与方法
1. 1
Matrigel:Becton Dickinson Compary, - 20 ℃保存;
Transwell plate:Costar ,USA , # 3422 ,聚碳酯膜微孔直径为8μm;
苏木素染液,梯度乙醇,二甲苯溶液。
1. 2 趋化因子的制备 取传代第二天长势良好的NIH3T3细胞,无血清培养基轻柔漂洗两次; 加入无血清培养基,37℃,5 %CO2 培养24 h~48h,收集细胞培养上清;4 ℃,12 000rpm 离心,10 min ,取上清;0.22 μm 滤膜过滤除菌;分装,在- 20 ℃保存。
1.3 transwell 培养板准备 所有操作均需无菌操作。-20℃保存的Matrigel 在冰上保2℃~8℃过夜融化。在冰上用预冷的枪头吸取100μl Matrigel 加入冰预冷的300μl 无血清培养基中,充分混均。取上述稀释的Matrigel 25 μl 加入transwell 板上室,覆盖整个聚碳酯膜,37 ℃,30 min ,使Matrigel 聚合成胶。已铺好Matrigel的transwell 培养板置于37℃可保存2 周。
1.4
Matrigel 侵袭实验(Matrigel Invasion Assay)刺激后的各组细胞用PBS 漂洗3 次。以常规方法用无血清培养基制备单细胞悬液,5 ×105个细胞/ ml ,每组细胞各分为两部分。胎盘兰拒染实验,细胞活力需大于95 %。Transwell 培养板上室加入100μl 细胞悬液( 5 ×104 个) 并加入无血清培养基200 ul 。Transwell 培养板下室加入500μl 趋化因子,37℃,5 %CO2 培养24 h。
用湿棉签轻轻擦去Matrigel 凝胶和聚碳酯膜上表面的细胞。小心取出上室,用线拴住,并做好标记,用冰预冷的甲醇固定30 min。苏木素染色1 min。
梯度乙醇脱水(80 % ,95 % ,100 %) ,二甲苯透明。小心将聚碳酯膜自上室基底切取下来,置载玻片上中性树脂封片。附着于聚碳酯膜下表面的细胞在高倍镜下( ×400) 随机取6 个视野[1 ] 计数,取平均数。重复实验两次。
